EAM Assessoria e Treinamentos no Processo Industrial e Segurança do Trabalho
Soluções de Problemas e Capacitação de Equipes
Princípios Básicos de Metalurgia para Desgaseficador à Vácuo RH
Objetivo:
Conhecer um pouco mais sobre os conceitos metalúrgicos do Processo de Refino no RH
Data de elaboração: 04 a 06 de abril de 2020
Índice
2.1 Reações de Desgaseificação.
2.8 Cinética do processo de Des-C.
2.9 O processo de Des-C nas unidades de RH.
3.0 Des-O de carbono ao vácuo (tratamento ligeiro)
3.6 Aplicação e uso de Lança de injeção.
3.7 Padrão de Tratamento para Descarburação Forçada.
3.8 Aquecimento Químico de Aços Desoxidados com aluminio.
3.9 Incremento de Temperatura com aluminio.
3.10 Aquecimento Químico de Graus ULC durante a Des-C do RH.
3.11 Injeção de Oxigenio para Prevenção de cascões.
3.12 Limitaciones Práticas para retirada de cascão.
4.0 Aplicações da Lança RH-OB.
1. Introdução: Tarefas e ferramentas para metalurgia secundária
As práticas convencionais de fabricação de aço no passado e antes da introdução de metalurgia de refino foram realizadas em unidades operacionais que incluíam fusão de cargas metálicas, reações de oxidação e reações de refino, como no caso da operação de fornos elétricos a arco, em outras unidades, como conversores de oxigênio, as temperaturas de esvaziamento foram aumentadas para realizar os ajustes necessários para atingir as condições de qualidade em serviço e cumprir as especificações. As consequências do exposto acima são longos tempos de fundição, longos períodos de refino e sujeição a condições extremas do equipamento de produção.
Hoje, a produção de aço é caracterizada por exceder os requisitos do cliente em relação às propriedades do material e a necessidade de o produtor de aço reduzir os custos de produção para permanecer competitivo no mercado mundial. Utilizando tecnologias modernas, a produção de aço foi dividida em processos de fusão e um estágio secundário de refino que torna a fabricação de aço mais econômica.
O objetivo do refino de aço secundário é aliviar o forno de fusão, transferindo o trabalho metalúrgico para a panela. As tarefas atuais dos fornos de fusão são a fusão da carga do metal, a desfosforização, a descarburação e o aquecimento do aço antes de ser esvaziado na panela de aço do refino. A temperatura de vazamento é baixa e prolonga o ciclo de vida do revestimento refratário e aumenta a produtividade.
O refino secundário do aço inicia-se durante o vazamento do aço com as primeiras adições de materiais e posteriormente as etapas de refino até atingir a desgaseificação do aço (desoxidação, dessulfuração, ajuste do aço e análise de escória, ajuste da temperatura do aço e homogeneização química e térmica).
Portanto, todas as plantas metalúrgicas de panela para tratamento de aço líquido, por exemplo, plantas metalúrgicas a vácuo, fornos de panela, injeção de argônio para agitação, instalações de injeção encapsulada são ferramentas usadas no refino secundário (Figura 1-1)
Fig. 1-1: Processos de metalurgia secundaria
1. Vantagens e Aplicações
Os processos de refino secundário são necessários nas modernas siderúrgicas, pois reduzem os custos de produção, aumentam a produtividade e permitem a produção de tipos de aço de alta qualidade. A aplicação de diferentes unidades secundárias de metalurgia é mostrada na Fig. 1-2.
As funções necessárias e as vantagens obtidas com o equipamento usado para tratamentos secundários de refino estão indicadas abaixo:
-
Introdução de gás de agitação inerte para homogeneizar o teor de aço.
-
Adição exata de elementos de liga, alcançando alto desempenho de liga e tolerâncias estreitas de composição química.Tratamiento de vacío para la remoción de hidrógeno, oxígeno, nitrógeno y carbón.
-
Injeções de materiais granulados, principalmente para fins de dessulfuração.
-
Alimentação de encapsulados como microconstituintes ou para controlar o tamanho da inclusão e melhorar a fundição do aço.
-
Aquecimento do aço com energia elétrica através de eletrodos de grafite ou como alternativa à energia química utilizando reação exotérmica de alumínio e oxigênio.
Figura 1.2 Aplicações da Metalurgia Secundária
1.3 Tratamento de Vácuo
Tratamento de Vácuo – uma Aplicação Especial de Metalurgia Secundária
As reações químicas que dependem da pressão do vácuo são a chave para remover certos elementos químicos indesejados do aço. Tais tratamentos a vácuo resultam na extração de elementos como carbono, oxigênio, hidrogênio ou nitrogênio do aço líquido.
Para que essas reações ocorram, o equilíbrio termodinâmico, a velocidade do fluxo de gás inerte e a cinética de transferência da fase líquida para a fase gasosa são fatores importantes.
Os seguintes benefícios econômicos podem ser esperados quando o equipamento secundário de refino estiver na linha de produção:
• Aumentos na produtividade da Aciaria.
• Reduções nos tempos da corrida dos fornos de fusão.
• Economia de energia e serviços.
• Uso de cargas de metal de baixo custo, bem como ferro-ligas.
• Qualidade consistente do aço entre corrida a corrida.
• Produção de aço ultra limpo.
• Desenvolvimento de novos tipos de aço.
• baixos custos de manutenção.
• Melhor coordenação de todas as unidades envolvidas na sequência de produção.
• Melhor condição de trabalho para a equipe operacional.
2.0. Metalurgia Básica
Termodinámica
As reações metalúrgicas são baseadas em leis da termodinâmica e cinética. A lei da termodinâmica bem compreendida e entendida significa o conteúdo de equilíbrio do estado final de uma reação química e a solubilidade dos elementos que entram em jogo. A cinética da reação refere-se ao tempo necessário para a transferência de massa do aço líquido para a fase gasosa até o estado final termodinamicamente definido da reação.
Essas relações também formam a base da metalurgia a vácuo, usada quando ocorre uma reação gasosa dos produtos, isto é, para remoção de hidrogênio, nitrogênio, descarburação e desoxidação a vácuo.
A redução da pressão de vácuo resulta na geração de produtos gasosos fora de equilíbrio químico. Esse processo, que se torna a força motriz básica da reação, continua até que um novo equilíbrio seja estabelecido com um menor teor de solubilidade em função da pressão final de trabalho.
Cinética
Como na maioria das reações químicas, o equilíbrio geralmente não é alcançado durante o tratamento a vácuo. Portanto, equações mais ou menos previsíveis são usadas para estimar o tempo necessário para o tratamento, capaz de descrever as etapas dos processos individuais da maneira mais precisa possível. Essas equações são derivadas empiricamente ou teoricamente ou são uma mistura de ambas as abordagens.
O estágio que define a taxa de remoção de hidrogênio, nitrogênio e descarburação ou desoxidação sob vácuo é decisivo para que a fórmula seja usada para determinar o tempo de tratamento. Essas sequências de estágios no tratamento a vácuo para a remoção dos elementos de interesse são as seguintes:
• O transporte dos elementos a serem removidos da frente de reação.
• A reação que ocorre, ou seja, no caso de hidrogênio e nitrogênio, a transição da forma atômica para a molecular ou, no caso de descarburação e desoxidação, a formação de monóxido de carbono.
• A remoção de produtos de reação.


2.1 Reações de Desgaseificação
Reações de Desgaseificação
A remoção de gases dissolvidos do aço líquido sob vácuo segue diferentes mecanismos de desgaseificação:
-
Nas pressões atmosféricas, existe um equilíbrio entre o hidrogênio na atmosfera e o hidrogênio dissolvido no aço, o que significa que o hidrogênio não pode ser removido. Quando a pressão do sistema é reduzida acima do nível do aço líquido, é gerado um desequilíbrio entre a fase gasosa e o aço líquido e, portanto, o hidrogênio pode ser removido por meio do equipamento de sucção.

-
Formação de bolhas de gás no aço líquido (nucleação homogênea), que significa a formação espontânea de uma bolha dentro do aço líquido. Esse comportamento ocorre porque é improvável que a energia de nucleação necessária ocorra no refino secundário.

-
Pre-Condicição Pgas > (pvac + ρSlag *g*hSlag + ρSteel*g* hSteel).
-
Formação de bolhas de gas em uma superfície de contato solida (Nucleação Heterogénea).
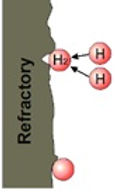
· Difusão de gas nas bolhas de saída do gás de argônio.

-
Formação de bolhas de gás, gotas de metal geradas no tratamento.
-
Pré condição: pGas > (pVac)
Dependendo de qual desses mecanismos é o predominante durante a desgaseificação, será a situação que temos nos processos de desgaseificação.
O conteúdo de hidrogênio e nitrogênio do aço fundido pode ser regulado por suas respectivas pressões parciais desses gases na atmosfera circundante.
De acordo com as investigações de A. Sieverts, a quantidade de hidrogênio ou nitrogênio dissolvido no metal é calculada pelas seguintes equações:

A solubilidade do hidrogênio em ferro puro a uma pressão parcial de hidrogênio de 1 bar e a uma temperatura de 1600 ° C é de 25 ppm [H]. A respectiva solubilidade do nitrogênio nas mesmas condições é de 450 ppm a 1 bar de pressão. Com pressão parcial de 1 mbar, o conteúdo é significativamente menor.

A Figura 2-1 mostra o conteúdo de equilíbrio de Nitrogênio e Hidrogenio para 1600 °C dependendo da pressão parcial de Pgas.

Figura 2-1: Conteúdos de Equilíbrio para [N] y [H] PARA 1600° C y pressão operativa
Em geral, o fluxo de massa entre gás e líquido é definido como

Onde:
-
D Constante de difusão.
-
Xe Concentração de equilibrio.
-
Xt Concentração no tempo t.
-
Espessura da interface de fase.
-
A Superficie de reação.
-
V Volume do aço.
-
C0 Concentração inicial.
A equação se aplica se ocorrer um processo de desgaseificação controlado, realizado por difusão. E este é o caso na remoção de hidrogênio e descarburação, e também na remoção de nitrogênio com muito baixo teor de oxigênio e enxofre.
Para permitir um uso prático desta equação, as seguintes variáveis
D, A e V estão agrupados no coeficiente de transferência de massa “k”. Este valor também é definido como a constante de velocidade, que representa o sistema – e tratamento – e parâmetros específicos durante o processo. Além disso, este é o fator determinante no cálculo do tempo de tratamento.
A forma da equação derivada da equação anterior é, com a nova expressão k:

A equação pode ser simplificada se a pressão for baixa, porque a influência da concentração de equilíbrio é desprezível. O resultado dessa simplificação é:

O, reorganizado:

-
t Tempo de tratamento
-
k Coeficiente de transferencia de massa
Essa fórmula geralmente é adequada para cálculos aproximados de concentrações ou tempos de tratamento e os mais comuns.